美國FDA批準Ardelyx的腎病相關藥物
http://www.libaolaser.com?? 2023-10-18 14:00 ??來源 溫州在線

美國FDA批準Ardelyx的腎病相關藥物
溫州網健康新聞訊,Ardelyx的藥物在最初被拒絕兩年多后于周二表示,美國食品和藥物管理局(FDA)已批準該藥物用于治療慢性腎病(CKD)患者的高磷酸鹽水平。
該藥物的品牌為Xphozah,被批準用于治療高磷血癥,這是一種導致血液中磷含量異常升高的疾病。
過量的磷會帶走骨骼和身體其他部位的鈣,進而導致骨骼脆弱、關節疼痛、肌肉痙攣和皮膚發癢。
FDA已批準該藥物用于對磷酸鹽結合劑療法反應不足或不耐受的患者,磷酸鹽結合劑療法是目前該病的標準治療方法。
該公司表示該藥物的商業上市正在進行中,并補充說預計將于11月上市。
Ardelyx在另一份聲明中表示,它已修改了與SLRCapitalPartners(SLR)管理的投資附屬公司的2022年債務融資協議,以獲得額外的5000萬美元,并可能進一步增加5000萬美元。
Ardelyx表示,預計將于10月份提取第二筆債務融資,以支持Xphozah的商業推出。
美國衛生監管機構于2021年拒絕批準Xphozah(化學名稱為tenapanor),理由是治療效果尚不清楚。在公司提出上訴后,它重新考慮并召開了顧問小組會議。
然而,FDA的外部顧問去年建議批準Xphozah作為單一療法或與現有療法一起治療透析患者的高血磷水平。
Xphozah屬于一類稱為磷酸鹽吸收抑制劑的藥物,其目標是腸道中負責磷吸收的蛋白質。
本文“美國FDA”來源:http://www.libaolaser.com/jiankang/jcdd/83781.html,轉載必須保留網址。編輯: yujeu
- 熱門內容
- 網友熱議
- 精彩內容

 同仁堂質量門 北京同
同仁堂質量門 北京同 擁有世界最大肱二頭
擁有世界最大肱二頭 浙江禽流感最新消息
浙江禽流感最新消息 江蘇禽流感最新消息
江蘇禽流感最新消息 大蒜的妙用 感冒吃大
大蒜的妙用 感冒吃大 h7n9診療方案 衛計委公
h7n9診療方案 衛計委公 美國FDA批準Ardelyx的腎
美國FDA批準Ardelyx的腎 美國FDA拒絕批準Alny
美國FDA拒絕批準Alny 墨西哥報告野鴨感染
墨西哥報告野鴨感染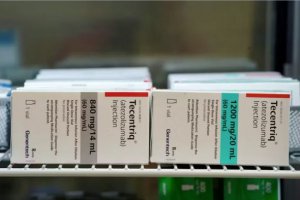 英格蘭將推出世界首
英格蘭將推出世界首